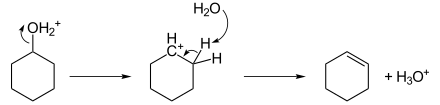
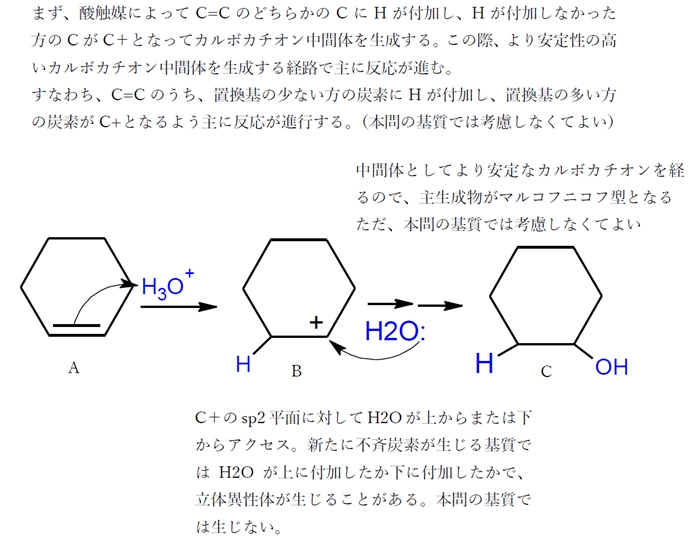
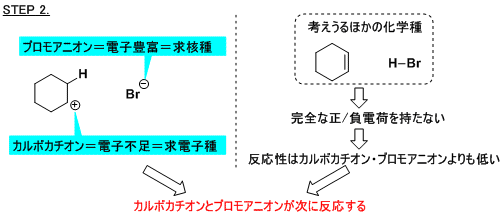
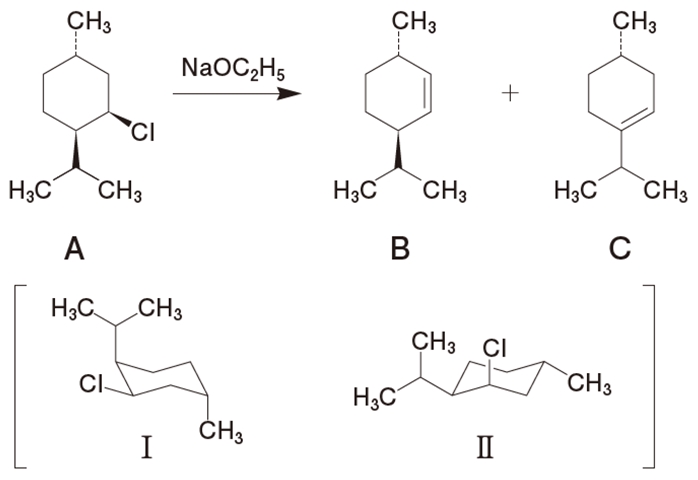
臭素価測定の検定用として、jis k 2605 にはシクロヘキセン(理論臭素価 187~199)および ジイソブテン(理論臭素価 136~144)が記載されています。シクロヘキセンは比較的臭素付加 反応が速いですが、ジイソブテンは遅いです。そのため終点条件(制御「シクロヘキセンへの臭化水素酸の付加反応」をとりあげます。この反応はどのような機構で起こっているのでしょうか?電子の矢印で反応機構を書くプロセスを、できるだけ詳細に解説してみます。 step 0 まず考えるべきは、どれとどれが反応するのか?問123 カルボカチオンを経る反応で,それぞれ以下の生成物が得られる.1メチルシク ロヘキセンから生じるカルボカチオンは第三級,シクロヘキセンから生じるそれは第二級 であるので,前者の方が速く反応する. (a) h 2 o 2 /n ao h (b) (c) c h h 3 c h h h br 2 c c h h 3 c h h h br 2 c h h3c h h

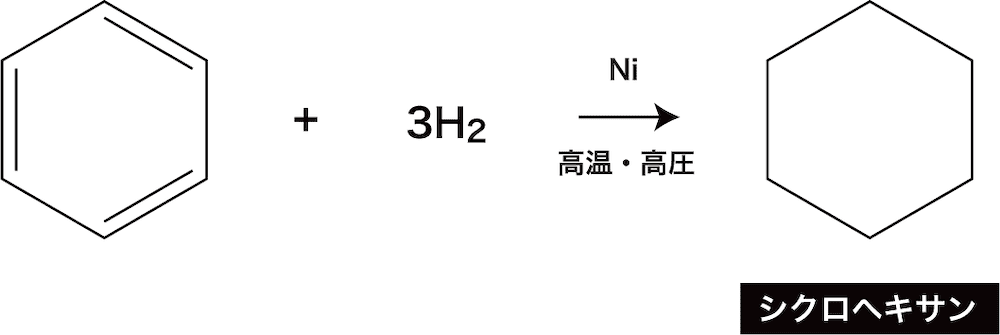
高校化学 ベンゼンの付加反応 映像授業のtry It トライイット
シクロヘキセン 臭素 反応式
シクロヘキセン 臭素 反応式-アルケンであるシクロヘキセンに臭素水を反応させると、茶褐色透明液が無色透明になります。これは、シクロヘキセン分子内の二重結合に臭素が付加することによります。 「動 画」臭素水にシクロヘキセンを加える 一般に二重結合を持つアルケンは、反応性が高いため様々な物質と反応し ヘキセンc6h12に臭素水を加えると, 付加反応が起こって,臭素の色が消えます。 左の試験管の上層がヘキサン。臭素の色が残っている。 右の試験管の上層はヘキセン。臭素の褐色は完全に消えている。 アルカンと臭素の反応は,光(紫外線)を当ててやると, 「置換反応」が起こります



有機化学の問題です メチルシクロヘキセンに水存在下で臭素を反応させる時臭 Yahoo 知恵袋
ヘキサンと臭素水の置換反応の化学反応式を教えてください! 0 回答 まだ回答がありません。 回答するにはログインが必要です。 ログインして質問に回答する 新規登録 疑問は解決しましたか? 解決した 解決しなかった この質問を見ている人は こちらの質問も見ています😉 化学 高校生問題12 次の反応式を完成させよ。なお、新たに立体が生じるものにはその立体化学が分 かる様に明記せよ。 br2 反応遷移状態 生成物 oso4 et2o 反応遷移状態 kmno4 生成物 h2so4/h2o 経由する反応中間体 生成物 oh o o h 経由する反応中間体 生成物 <解説> シクロヘキセンを臭素化する際はブロムAd疫情持续政策变,加一帮您渡难关 把握时机报读加一思培保證班, 考过思培, 完成移民梦 加一思培线上课程由官方认證老师授课 在家就能轻松提高考试技巧,请即联繫我们查询报名
問シクロヘキセンの臭素付加反応について、生成物を構造式で表せ。 答えと解説を宜しくお願いします。 空前絶後のぉー 超絶怒涛のぉー 超簡単基礎問題 回答するのも恥ずかしい なので回答がつかないのだろぅ 諦めて教科書でも読めば?シクロヘキセン 別名 テトラヒドロベンゼン、(Tetrahydrobenzene) 分子式 (分子量) C6H10(14) 化学特性 (示性式又は構造式) CAS番号 1108 官報公示整理番号(化審法・安衛法) (3)2234 分類に寄与する不純物及び安定化添加物 データなし 濃度又は濃度範囲 100%化学式C6H10 化学名重量 反応性データなし 化学的安定性光により変質するおそれがある。 シクロヘキセン1000 00 mg/kg ( Rat )> 162 mg/kg ( Guinea pig ) N/A 化学名 急性毒(経口)分類根拠皮吸入ガス シクロヘキセンNITEのGHS分類に基づく。NITEのGHS分類に基づく。NITEのGHS分類に基づく。 化学名 急性
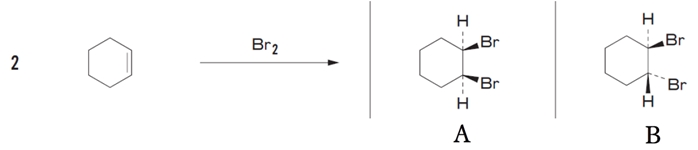
アルケンへの付加反応 その2 共役化合物 19年6月14日 第8回 有機反応化学 1 まずは前回の復習! 2 アルケンへの付加反応 付加反応の例 ★ 3 反応機構が一番分かりやすいhxの付加反応からやる 二段階の反応機構 1.アルケンへのプロトン付加 → カルボカチオンが生成 2.ハロゲン化物イオン(x 反応機構 実際に臭素供与体として働くのは、系中で極微量生じているbr 2 であり、nbsではないことに注意。臭素が大量に存在している場合、副反応が避けられない。10 シクロヘキセンに次のような付加反応を行った。得られる主生成物が、ラセミ体とな るものはどれか。2つ選べ。ただし、立体配座異性体は考えないものとする。解答:1,3 1 臭素を反応させたときの生



シクロヘキセンからtrans 1 2 シクロヘキサンジオールを効率 Yahoo 知恵袋



シクロヘキセン Wikipedia
次の表は、シクロアルケンの最も重要な反応を示しています。 二重結合を有する炭素の1つがラジカルで置換されている場合、反応物から来る水素は、最大数の水素原子を有する炭素と結合する。これはマルコフニコフ則と呼ばれます 例 シクロヘキセン:C 6 H 10 シクロブテン:C 4 H 6 シクロペンテシクロヘキセンの臭素価 関連業種 石油 使用装置 電位差自動滴定装置 測定手法 定電流分極滴定 関連規格 jis k2605 「jis k2605 石油製品-臭素価試験方法-電気滴定法」に基づき定電流分極滴定によりシク ロヘキセンの臭素価を測定しました。めに立体化学を含めて説明する。例えば(1)式に示すよう に,シクロペンテンへの臭素の付加反応は,trans 1,2ジ ブロモシクロペンタンを与える。 アルケンへの臭素の付加反応は,2段階で進行して



1



アルケン 求電子付加反応 総合問題 ラセミ体 91回問7a D
(6)下線部ⅳ)において,シクロヘキセンと臭素が反応すると,二重結合に臭素が付加し た生成物が生じる。シクロヘキセン41.0mg が完全に臭素と反応すると,得られる生 成物は何mg か。有効数字3桁で記せ。 ―11― ロビンソン構造式の方が本質的であることを、 エネルギー的にも確認しておきましょう。 このように、 シクロヘキセンに水素を付加した時の熱は約1kJ、 1,3シクロヘキサジエンに水素を付加した時の熱は約230kJです。 つまりベンゼンがケクレ構造式であるシクロヘキセンに次の反応eを行った。 得られる主生成物がラセミ体となるか判定してみよう。ただし、立体配座異性体は考えないものとする。 e mクロロ過安息香酸を反応させたときの生成物に、 さらに酸触媒による加水分解反応を行ったときの生成物 トップページへ 薬剤師国家試験過去



芳香族炭化水素




ウォール チーグラー臭素化 Wohl Ziegler Bromination Chem Station ケムステ
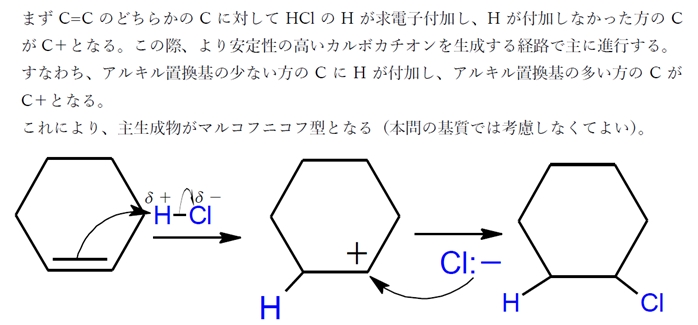
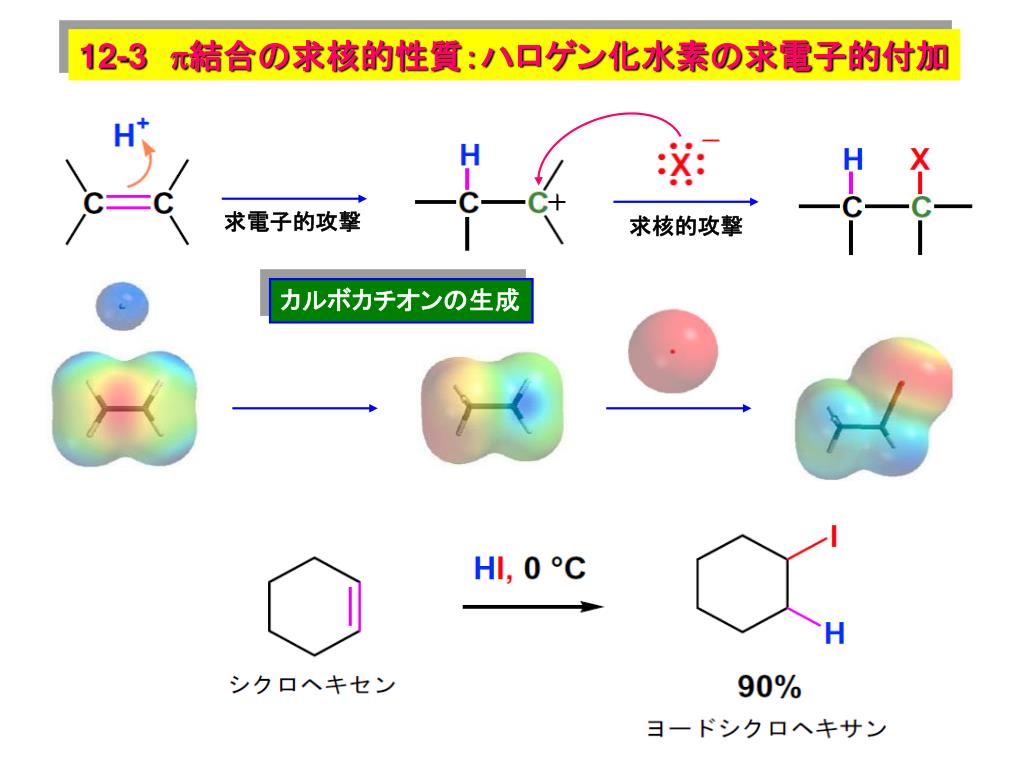
また塩素(Cl 2 )や臭素(Br 2 )などのハロゲンもラジカル反応の例として頻繁に出されます。ハロゲンに熱または光(紫外線・UV)を与えることで、結合が開裂してラジカルが作られます。反応の種類 どんな反応か 特徴 ホモリシス ラジカルの 数が増える ラジカル カップリング ラジカルの 数が減る 原子引き抜き σ結合が切れて 新しいσ結合が できる 二重結合への ラジカルの付加 二重結合が なくなる β開裂 二重結合が Cできる C R RC C RC C C C R RA–R' R–AR' RR R–R R–R RR ラジカル反応の分類 4アルケンの反応 ハロゲンの付加 教科書p 538p ~545 ハロゲンの付加 臭素化反応 水素化反応 シン(syn)付加 H I の付加 カルボカチオン中間体 立体特異的反応 ラセミ体 2 2 アンチ(anti)付加 エナンチオマー ラセミ体 ジアステレオマー メソ体 臭素化(反応機構) δ(デルタプラス
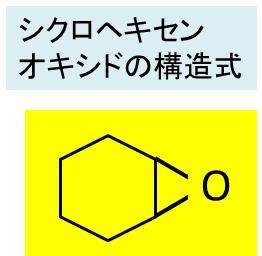



シクロヘキセンオキシド C6h10o の構造式は 水と反応し開環が起こる




10 号 不飽和脂環式ポリカルボナート及びその製造方法 Astamuse
ヘキセン-1(Hexene1) 化学式: C 6 H 12 化学特性(化学式又は構造式): CAS番号: 官報公示整理番号 (2)22 (化審法・安衛法): 分類に寄与する不純物及び安定化添加物: 情報なし 濃度又は濃度範囲: 97%以上 4.応急措置 吸入した場合: 被災者を新鮮な空気のある場所に移動臭素と反応して1,2ジブロモシクロヘキサンを形成する過マンガン酸カリウム(KMnO)の存在下で急速に酸化する 4 )ペルオキシ安息香酸の存在下でエポキシド(シクロヘキセンオキシド)を生成することができる。 合成1 シクロヘキセンと60%硫 酸との反応 硫酸/ chの モル比1,反 応温度500cで 反応時間を変えて反 応を行ないno1の 収率に及ぼす反応時間の影響につい て検討した。その結果を図2に 示した。反応8時 間まで はno1お よびシクロヘキサン酸性硫酸エステル(chs)



芳香族炭化水素



シクロヘキセン 臭素 シクロヘキセン 臭素 化学反応式 Takuminanasekiwakimlj
アルケンと臭素の反応:第二段階 C–Br 背面攻撃 (backside attack) (脂肪族求核置換反応 (SN2) でもう一度出てくる) C C H3C H H H3C Br– Br C C H3C H H CH3 Br Br 6ンの水素化反応をシクロヘキセンで止める 部分水素化反応は極めて困難であった。 この困難さを克服したもの、即ち本技術 の重要な特徴の一つが、その反応場にある。 反応は液相で行うが、図 4 に示すように、 系は気相(水素)-油相(原料及び生成物) -水相-固体(触媒など)の4Ad疫情持续政策变,加一帮您渡难关 把握时机报读加一思培保證班, 考过思培, 完成移民梦 加一思培线上课程由官方认證老师授课 在家就能轻松提高考试技巧,请即联繫我们查询报名



アルケン 臭素 ハロゲン 付加 アンチ付加 98回問103の2



放浪者の道標 基礎有機化学 16 アンチ付加
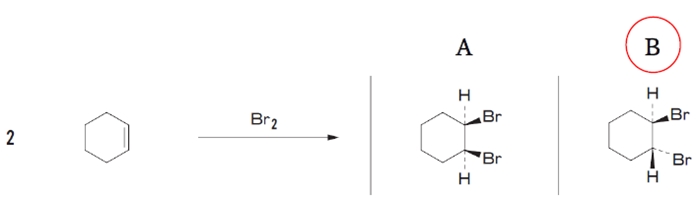
例:シクロヘキセン 例:シクロヘキサン シクロ (脂環式炭化水素) シクロアルケン(脂環式炭化水素) 例:ベンゼン c c c c h h ・化学の計算問題は,物質量を基準にして考えることがポイントとなる! ・質量から物質量,物質量から質量の変換がすぐにできるようシクロヘキセンはcの式 を たとえば、臭素を使用すると、求電子的に付加されます。 シクロヘキサンとシクロヘキセンの違いは何ですか? シクロアルカンは、環構造の炭素原子間に単一の共有結合のみを持つ有機化合物です。シクロヘキサンは良い例です。一方、シクロアルケンは、環構造 1.ます臭素分子がシクロヘキセンの二重結合に接近して、鎖体を形成します。 2.次に二重結合にBrが付加して3員環のブロモニウムイオンになる。 3.Br付加した方と反対側からBrが付加する。 3ゆえにトランス体になります。なので生成物はtrans12ジブロモシクロヘキサン 図は下記の臭素の付加参照(手抜きですみません)
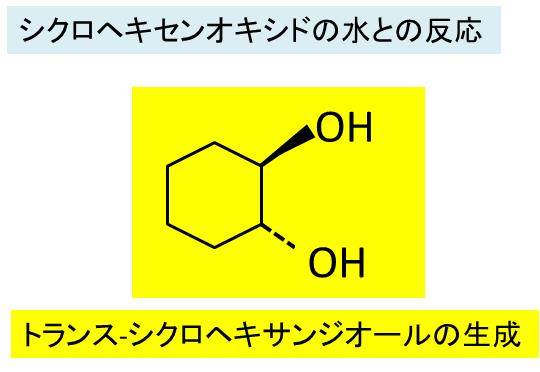



シクロヘキセンオキシド C6h10o の構造式は 水と反応し開環が起こる




高校化学 ベンゼンの付加反応 映像授業のtry It トライイット
ウォール・チーグラー反応はNBSを用いたアリル位、ベンジル位選択的な臭素化反応です。 1919年にA WohlによりNブロモアセトアミドによるアルケンの臭素化が発見され、1942年K ZieglerはNブロモスクシンイミド(NBS)を用いたアリル位臭素化を行い、さらにPKarrerにより触媒量の過酸化ベンゾイル $$反応速度 = k(CH_3)_3CClOH^(mol*L^{1}*s^{1})$$ この式はS N 2反応の反応速度式と同じ形をとっています。 すなわち、基質から脱離基が脱離してカルボカチオンが生成する前に、求核剤が基質に対して攻撃してしまうのです。5 反応の自由エネルギーは,平衡定数kから以下の式に従って計算できる。 7 このディールズ-アルダー反応では,スチレンの芳香族性のもとになっているπ共役系は 完全に損なわれる。生成物はもはや芳香族性を示さない。結果的に共鳴安定化エネルギー




シクロヘキサンとシクロヘキセンの違い 類似用語の違いを比較する 理科 22




高校化学 ベンゼンの付加反応 映像授業のtry It トライイット
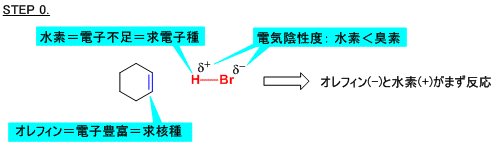



反応機構を書いてみよう 電子の矢印講座 その2



芳香族炭化水素



Sci Kumamoto U Ac Jp



1




理科実験のページ 埼玉県立松山高等学校




ラジカル反応 ホモリシスや連鎖反応 位置選択性の反応機構 リョースケ大学
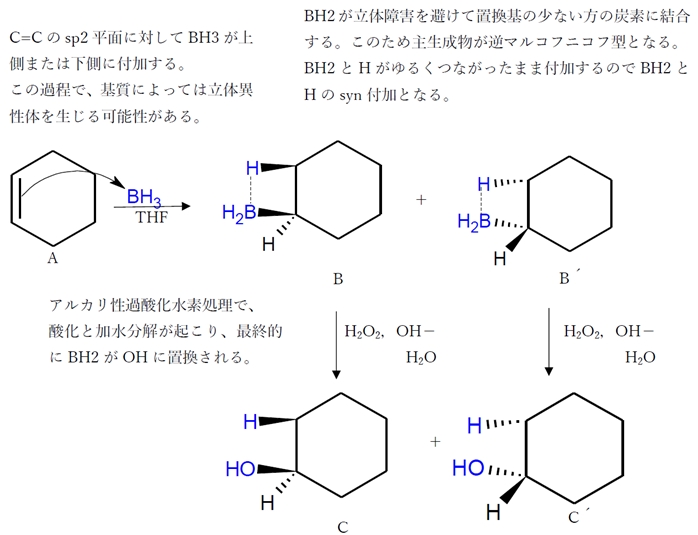



アルケン 求電子付加反応 総合問題 ラセミ体 91回問7a D




シクロヘキセン Wikipedia
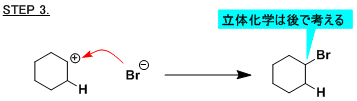



反応機構を書いてみよう 電子の矢印講座 その2



有機化学の問題です メチルシクロヘキセンに水存在下で臭素を反応させる時臭 Yahoo 知恵袋




1 3 5 シクロヘキサトリエン Wikipedia




15 号 二酸化炭素とエポキシドとの共重合のための二金属触媒錯体 Astamuse



アルケン 求電子付加反応 総合問題 ラセミ体 91回問7a D




Eureka 11 有機化学反応ってどうやって起こっているの 例題を元にプロセスを追ってみよう



1 メチルシクロヘキセンに 酢酸中hbrを反応させたときの生成物の構造 Yahoo 知恵袋



アルケン 臭素 ハロゲン 付加 アンチ付加 98回問103の2



第67章 実験 液体の炭化水素



有機化学が理解できる方 おられますか シクロヘキセンへの臭素付加 Yahoo 知恵袋



コンプリート シクロヘキセン 臭素 化学反応式 シクロヘキセン 臭素 化学反応式 Mbaheblogjpdjag
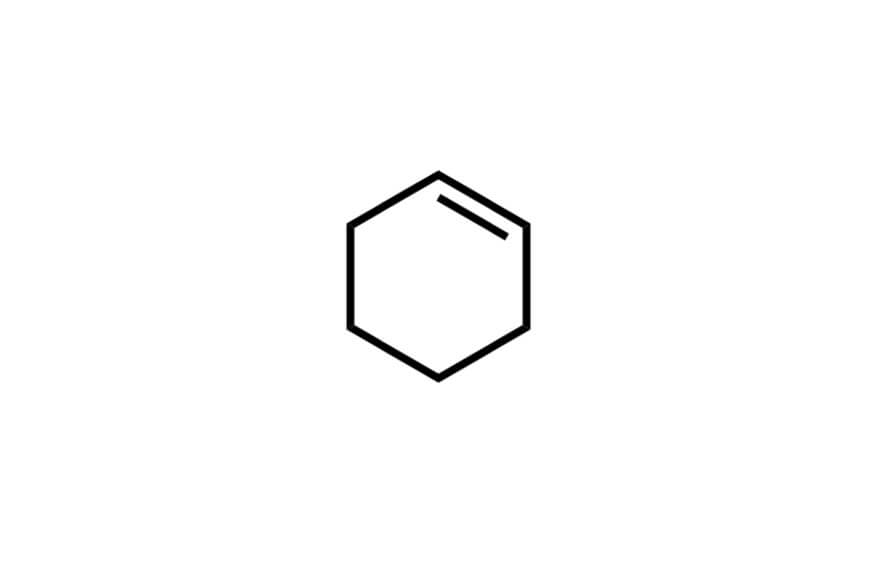



シクロヘキセン



高等学校のコンテンツ



シクロヘキセン C6h10 の化学式 分子式 構造式 電子式 示性式 分子量は




19 の解答はの構造式はシクロヘキセンですか シクロペンタンに見えます 同 Clearnote



高等学校のコンテンツ



第67章 実験 液体の炭化水素




ウォール チーグラー臭素化 Wohl Ziegler Bromination Chem Station ケムステ




号 3座配位子を有する鉄錯体化合物及びその製造方法 並びに有機ボロン酸エステルの製造方法 Astamuse



芳香族炭化水素



脂肪族炭化水素 ジエンの特徴 技術情報館 Sekigin 共役ジエンの特徴に関し 二重結合を 2 つもつジエンの構造と分類 共役系の定義と安定性 共役ジエンの求電子付加反応の特徴 ディールス アルダー付加環化反応を 紹介



コンプリート シクロヘキセン 臭素 化学反応式 シクロヘキセン 臭素 化学反応式 Mbaheblogjpdjag




コンプリート シクロヘキセン 臭素 化学反応式 シクロヘキセン 臭素 化学反応式 Mbaheblogjpdjag




アルケンへの臭素付加 らくらく理科教室



高等学校のコンテンツ



Ppt 12 章 アルケンの反応 Powerpoint Presentation Free Download Id



1 Methyl 1 Cyclohexene 591 49 1 Tci Europe N V



1



シクロヘキセンに 四塩化炭素中 Br を反応させたときの生成物の構造式を そ Yahoo 知恵袋




シクロヘキセン Wikipedia



ブロモシクロヘキサン



高等学校のコンテンツ



反応機構を書いてみよう 電子の矢印講座 その2



1




コンプリート シクロヘキセン 臭素 化学反応式 シクロヘキセン 臭素 化学反応式 Mbaheblogjpdjag



くさいもと 臭素を使った実験



2k基礎有機 章末問題こたえ



Www2 Meijo U Ac Jp



Gipc Akita U Ac Jp
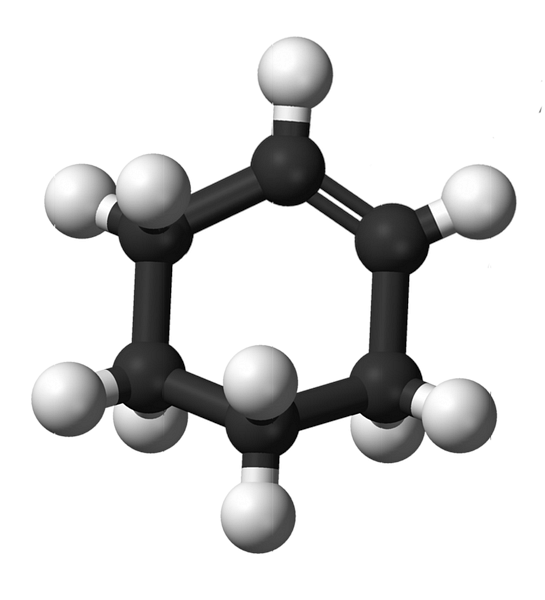



シクロヘキセンの構造 性質 合成および用途 化学 Thpanorama 今日自分を良くする
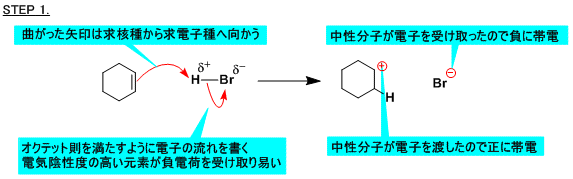



反応機構を書いてみよう 電子の矢印講座 その2



Chem S U Tokyo Ac Jp




シクロヘキセン 臭素 シクロヘキセン 臭素 化学反応式 Takuminanasekiwakimlj



有機化学が理解できる方 おられますか シクロヘキセンへの臭素付加 Yahoo 知恵袋



脂肪族炭化水素 ジエンの特徴 技術情報館 Sekigin 共役ジエンの特徴に関し 二重結合を 2 つもつジエンの構造と分類 共役系の定義と安定性 共役ジエンの求電子付加反応の特徴 ディールス アルダー付加環化反応を 紹介



コンプリート シクロヘキセン 臭素 化学反応式 シクロヘキセン 臭素 化学反応式 Mbaheblogjpdjag




この物質に直接臭素を反応させてもa位は臭素化できないのでしょうか Okwave



有機化学の反応の主生成物の構造式を求める問題で 質問です 添 Yahoo 知恵袋




化学センター試験解説 Kumonotaira




化学式 その6 ベンゼンとシクロヘキサン 薬剤師を目指す学生と甘味料系少女のブログ



1




高等学校化学i 炭化水素 環式炭化水素 Wikibooks
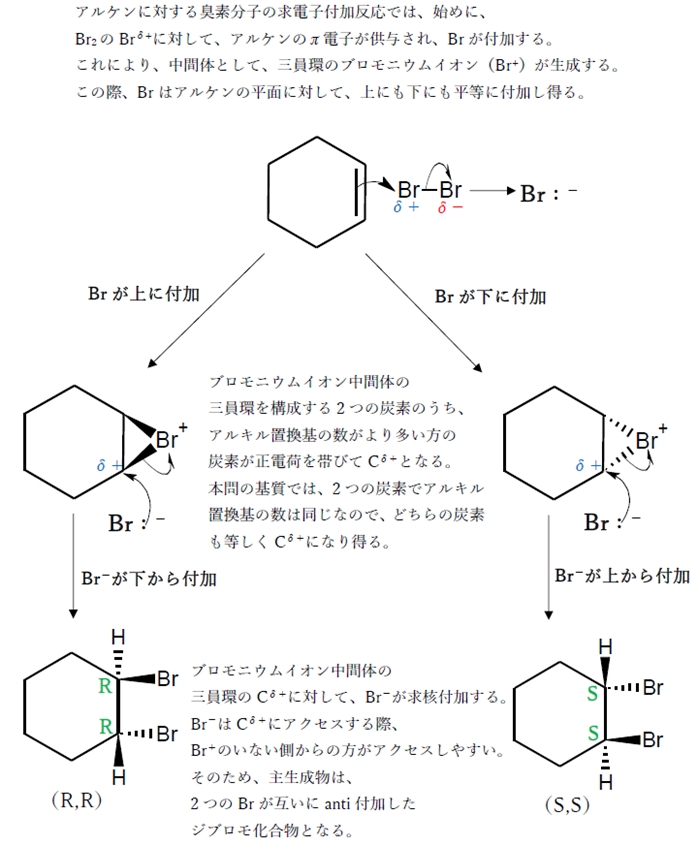



アルケン 臭素 ハロゲン 付加 アンチ付加 98回問103の2



ベンゼン 構造 特徴 製法 各種反応など 化学のグルメ
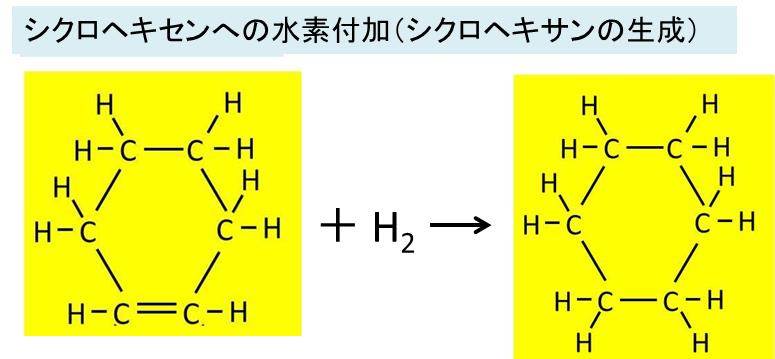



シクロヘキセン C6h10 の化学式 分子式 構造式 電子式 示性式 分子量は




シクロヘキセンオキシド構造の意味 用法を知る Astamuse



ハロゲン化シクロヘキサンのe2脱離 総合問題 104回問101




環式炭化水素と臭素水 Youtube
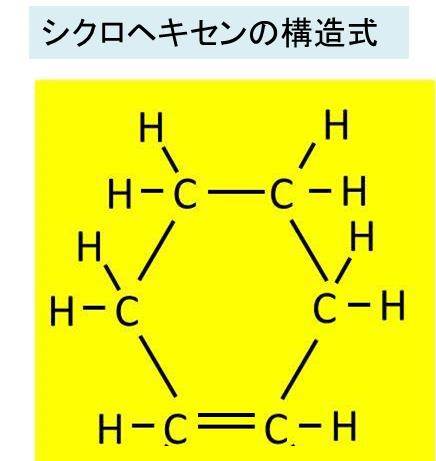



シクロヘキセン C6h10 の化学式 分子式 構造式 電子式 示性式 分子量は



1




有機化学 アルケン アルキンへのラジカルの付加 Br メチルヘキセン 臭素 共鳴 構造 Ccl4 Nbs 東京グルメ紀行



1 5 ジメチルシクロヘキセン 化学物質情報 J Global 科学技術総合リンクセンター




メチルシクロヘキサン Wikipedia



放浪者の道標 基礎有機化学 16 アンチ付加



3 メチル 5 プロピル 2 シクロヘキセン 1 オン 37 16 9




02 号 アミノシクロヘキシルエーテル化合物およびその用途 Astamuse




4 Methyl 1 Cyclohexene 591 47 9 Tci Europe N V



問題7 15 C の1 メチルシクロヘキセンと3 メチルシクロヘキセンのど Yahoo 知恵袋




脱離反応 E1反応 E2反応の違いや二重結合を作る反応機構 リョースケ大学



Chem S U Tokyo Ac Jp
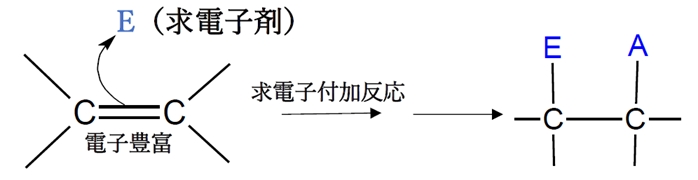



アルケン 求電子付加反応 総合問題 ラセミ体 91回問7a D



1 ニトロ 1 シクロヘキセン 化学物質情報 J Global 科学技術総合リンクセンター




高校化学 ベンゼンの付加反応 映像授業のtry It トライイット



放浪者の道標 09年07月



Ek U Tokai Ac Jp
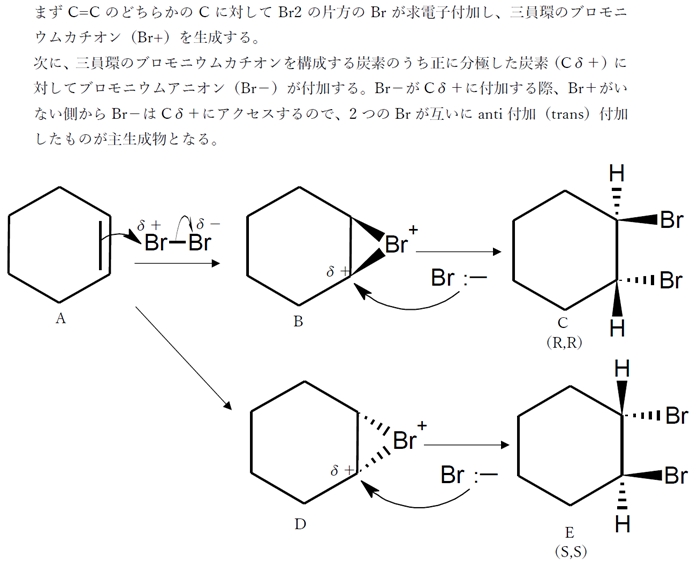



アルケン 求電子付加反応 総合問題 ラセミ体 91回問7a D




19 の解答はの構造式はシクロヘキセンですか シクロペンタンに見えます 同 Clearnote




臭素の付加反応 Z および E 2 ブテンへの臭素の付加反応におい Okwave




シクロヘキサンとシクロヘキセンの違い 類似用語の違いを比較する 理科 22



Chem S U Tokyo Ac Jp



0 件のコメント:
コメントを投稿